MINIGUÍA PARA PACIENTES
Monográfico sobre la Mácula: Anatomía, Fisiología, Patofisiología y Avances Clínicos
INTRODUCCIÓN
La mácula, una región especializada de la retina de 5-6 mm de diámetro, es fundamental para la visión de máxima agudeza visual, la percepción del color y la estabilidad de la fijación. Su importancia clínica radica en su susceptibilidad a enfermedades como la degeneración macular asociada a la edad (DMAE), el edema macular diabético (EMD) y las distrofias hereditarias de la retina, que son causas principales de ceguera en poblaciones adultas. En 2020, se estimó que la DMAE afectaba a 196 millones de personas a nivel mundial, con proyección de aumento a 288 millones para 2040 ( Global Prevalence ). Los avances en técnicas de imagen, como la OCT, la OCT-A, la autofluorescencia y la tomografía de coherencia óptica (OCT) asistida por inteligencia artificial (IA), y en tratamientos, como la terapia génica, han transformado el manejo de estas patologías. Este monográfico profundiza en la relevancia de la mácula, y de sus enfermedades destacando su impacto socioeconómico y los desafíos clínicos actuales.
IMPORTANCIA CLÍNICA
La DMAE es la principal causa de ceguera legal en adultos mayores en países desarrollados, representando el 8.7% de la ceguera global. Las distrofias maculares, como la enfermedad de Stargardt, afectan a poblaciones más jóvenes, impactando en la calidad de vida desde edades tempranas (infancia y juevntud). La carga económica de estas enfermedades es significativa, con costos asociados a tratamientos crónicos y a rehabilitación visual.
Avances recientes:
La integración de IA (inteligencia artificial) en el análisis de imágenes OCT ha mejorado la detección temprana de cambios patológicos, mientras que la óptica adaptativa permite visualizar las células individuales en la retina ( AI Retinal Imaging ). Las terapias anti-VEGF de nueva generación, como el Faricimab, y las terapias génicas, como el ABBV-RGX-314, ofrecen opciones menos invasivas y más duraderas ( Gene Therapy ).
ANATOMÍA DE LA MÁCULA
La mácula se caracteriza por una alta densidad de conos, una estructura avascular en la fóvea y una disposición única de células que optimizan la transmisión de los fotones. A continuación, detallamos la ultra-estructura de la mácula, incluyendo las células de Müller, las fibras de Henle, el epitelio pigmentario retiniano (EPR) y los pigmentos maculares.
2.1 Ultra-estructura
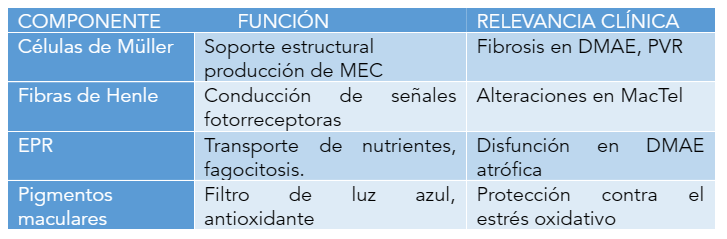
- Células de Müller: Estas células gliales principales atraviesan toda la retina, proporcionando soporte estructural y actuación a través de canales como TRPV4 y Piezo1. Producen componentes de la matriz extracelular (MEC), como colágenos y proteoglicanos, que son esenciales para la estabilidad retiniana ( Müller Glia ).
- Fibras de Henle: Compuestas por axones de fotorreceptores no mielinizados y procesos de células de Müller, estas fibras contribuyen a la arquitectura radial de la mácula. Estudios recientes han identificado su ensamblaje por microglías en condiciones patológicas, como en el caso de la telangiectasia macular tipo 2 ( MacTel Analysis ).
- Epitelio Pigmentario Retiniano (EPR): El EPR, adherido a la membrana de Bruch, desempeña un papel crítico en el transporte de nutrientes y la eliminación de desechos. Su disfunción está implicada en la DMAE seca ( Análisis MacTel ).
Pigmentos maculares : La luteína, la zeaxantina y la meso-zeaxantina se concentran en la mácula, filtrando luz azul y actuando como antioxidantes ( macular pigments ).
2.2 Imagen de alta resolución
La óptica adaptativa combinada con OCT ( imagen de OCT mejorada con óptica adaptativa) permite visualizar capas maculares con resolución celular, revelando cambios tempranos en enfermedades como la DMAE ( Adaptive Optics ).
FISIOLOGÍA DE LA MÁCULA
La mácula es esencial para la visión de alta agudeza, la percepción del color y la estabilidad de la fijación. Esta sección ampliada explora los mecanismos de fototransducción, el papel de los pigmentos maculares y la influencia de los ritmos circadianos.
Fototransducción
La fototransducción en los conos implica la absorción de luz por opsinas, desencadenando una cascada que modula la liberación de glutamato. Los conos de la mácula, con fotopigmentos específicos (eritrolabio, clorolabio, cianolabio), son responsables de la visión fotópica (Circadian Phototransduction ).
Pigmentos maculares
La luteína, zeaxantina y meso-zeaxantina absorben luz azul (pico a 460 nm) y neutralizan las especies reactivas de oxígeno (ROS). Su estructura química, con grupos hidroxilo, les permite cruzar barreras hematorretinianas, protegiendo las células retinianas ( Macular Pigments ).
Ritmos circadianos
Los marcadores moleculares en la retina, regulados por genes como CLOCK y BMAL1, influyen en la función macular. Las disrupciones circadianas aumentan el estrés oxidativo, un factor que parece jugar un papel clave en la DMAE ( Circadian Rhythms ).
“Los ritmos diarios son una característica común de los sistemas vivos. Generalmente, estos ritmos se originan dentro del organismo y se sincronizan con las fluctuaciones cíclicas del entorno externo. Los mamíferos poseen una red corporal de relojes circadianos endógenos con un período de entre 20 y 28 h.”
PATOFISILOGÍA MACULAR
Las enfermedades maculares, como la DMAE, la EMD y las distrofias hereditarias, tienen bases moleculares y genéticas complejas. Esta sección ampliada detalla los mecanismos patogénicos, biomarcadores y ensayos clínicos recientes.
Degeneración Macular Asociada a la Edad (DMAE)
- Mecanismos: La DMAE atrófica se caracteriza por la presenciade drusas, cambios en el EPR de la retina y atrofia geográfica, mientras que la DMAE neovascular implica neovascularización coroidea producida por la activación del VEGF. La disregulación de la vía del complemento (CFH, C3) está implicada en la patogénesis de la DMAE atófica ( AMD Genetics ).
- Biomarcadores: La densidad de pigmento macular, las lesiones hiperreflectivas y el volumen de las drusas son indicadores pronósticos de la enfermedad o biomarcadores ( AMD Biomarkers ).
Edema macular y distrofias
El EMD resulta de la rotura de la barrera hematorretiniana, mientras que las distrofias retinianas como el Stargardt están asociadas con mutaciones en genes como el ABCA4 ( Macular Dystrophies ).
Ensayos clínicos
Ensayos recientes han evaluado Faricimab ( Vabysmo) para la DMAE Neovascular y Pegcetacoplan ( Syfovre) para la atrofia geográfica, mostrando reducciones significativas en el crecimiento de lesiones ( Clinical Trials ).
EVALUACIÓN CLÍNICA Y DIAGNÓSTICA
La evaluación de la mácula se basa en técnicas de imagen multimodal avanzadas, como la OCT, la microperimetría, la autofluorecencia y la angiografía por OCT (OCT-A), aumentadas mediante IA y por la óptica adaptativa.
Comparación de plataformas OCT
- SD-OCT (spectral domain) vs. SS-OCT (swept source) : SS-OCT ofrece mayor profundidad de penetración y velocidad, mejorando la visualización de la coroides ( Comparación OCT ).
- OCT-A:Detecta el flujo vascular sin contraste, útil para los casos de neovascularización coroidea ( AI OCT ).
Inteligencia Artificial
La IA mejora la segmentación de imágenes OCT, prediciendo la progresión de la DMAE con AUC de 0.745-0.96 ( AI OCT Analysis ).
Óptica Adaptativa
La óptica adaptativa permite visualizar las células individuales, como en el EPR, mejorando el diagnóstico temprano ( Adaptive Optics ).
TRATAMIENTOS Y PERSPECTIVAS FUTURAS
Los tratamientos para las enfermedades maculares han evolucionado desde inyecciones anti-VEGF hasta la terapia génica y regenerativa.
Anti-VEGF de nueva generación
Faricimab, un anticuerpo bioespecífico, reduce la frecuencia de inyecciones IV a un periodo de 16 semanas, mejorando la adherencia al tratamiento ( Vabysmo ).
Terapia génica
ABBV-RGX-314 utiliza vectores AAV8 para producir proteínas anti-VEGF, eliminando la necesidad de inyecciones repetidas ( Gene Therapy ).
Terapias regenerativas
El trasplante de células madre derivadas de EPR ha mostrado mejoras en la agudeza visual en ensayos de fase 1/2a ( Stem Cell ).
CASOS CLÍNICOS ILUSTRATIVOS
Aunque los informes de casos específicos son limitados, los datos de ensayos clínicos proporcionan ejemplos ilustrativos.
Caso de DMAE seca
Seis pacientes con DMAE atrófica tratados con RPESC-RPE-4W (50.000 células) mostraron una mejora promedio de 21,67 letras en la agudeza visual a los 12 meses ( Luxa Biotech ).
Caso de DMAE húmeda
Pacientes tratados con Faricimab en ensayos de fase 3 mantuvieron la visión con inyecciones administradas cada 16 semanas, con reducciones significativas en el espesor macular ( Clinical Trials ).
PERSPECTIVAS FUTURAS Y LÍNEA DE INVESTIGACIÓN
Las tecnologías emergentes están transformando el manejo de las enfermedades maculares.
Inteligencia Artificial
La IA mejora la predicción de la progresión de la DMAE, con modelos que alcanzan AUC de hasta 0,96 ( AI OCT ).
Óptica Adaptativa
La combinación de óptica adaptativa con OCT permite imágenes de resolución celular, detectando cambios tempranos en el EPR (AI Adaptive Optics ).
Nanotecnología
Aunque en etapas incipientes, la nanotecnología promete sistemas de administración de fármacos de liberación prolongada, reduciendo la frecuencia de las inyecciones ( Macular Breakthroughs ).
CONCLUSIONES
La mácula sigue siendo motivo de innovación en oftalmología, con avances en Imagen multimodal, terapias génicas y regenerativas que mejoran los resultados clínicos. La integración de IA y de la óptica adaptativa promete diagnósticos más precisos, mientras que las terapias de larga duración reducen la carga para los pacientes y para el sistema de salud, público y privado. La investigación futura debe centrarse en tratamientos personalizados y estrategias de prevención.
BIBLIOGRAFÍA
- Prevalencia mundial de la degeneración macular relacionada con la edad 2020-2040
- La IA hace que la obtención de imágenes de retina sea 100 veces más rápida
- Beneficios de la terapia génica para la degeneración macular
- Función de la glía de Müller en la matriz extracelular de la retina
- Análisis ultraestructural de la telangiectasia macular tipo 2
- El papel del pigmento macular en la protección de la retina
- Modelado de la fototransducción circadiana en la retina
- Alteración del ritmo circadiano y fisiopatología retiniana
- Nuevos tratamientos y genética de la DMAE
- Análisis OCT basado en IA para la progresión de la DMAE
- Compatibilidad de IA con OCT en AMD
- Óptica adaptativa en enfermedades hereditarias de la retina
- Descripción general de la prueba ocular OCT
- Intervención de terapia génica en la enfermedad ocular neovascular
- Avances en la investigación de la DMAE y ensayos clínicos
- Actualización del ensayo clínico de marzo de 2024
- Trasplantes de células madre para la DMAE seca
- Características clínicas y genéticas de las distrofias maculares
- Imágenes de retina con resolución celular asistidas por IA
- Tratamientos emergentes para la degeneración macular
- Oftalmoscopia con óptica adaptativa para la DMAE
Dirección
Av. San Francisco Javier, 9, 41018 Sevilla